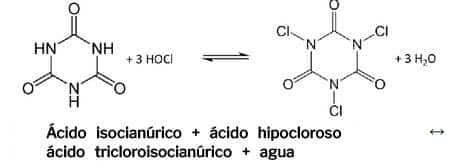
El ácido cianúrico (CYA) es una herramienta útil para estabilizar los residuos de cloro y reducir la degradación del cloro por la radiación UV de la luz solar. La mayor mejora en la retención de cloro se observa con la adición de los primeros 5 ppm de CYA. Se observan rendimientos decrecientes en la estabilización UV a medida que aumenta la concentración de CYA, particularmente en concentraciones de CYA entre 20 ppm y 100 ppm, donde los incrementos de CYA muestran poca mejora incremental en la estabilización de los residuos de cloro.
Si bien el CYA es una química útil para reducir la degradación del cloro por la radiación UV de la luz solar, la interacción del CYA con el residuo de cloro ralentiza la tasa de desinfección del cloro, disminuye el ORP e inhibe la actividad del cloro contra las algas. Debido a esto, el uso de CYA debe ser limitado.
Para piscinas interiores, la degradación del cloro por la radiación UV de la luz solar es mínima, por lo que no se debe utilizar CYA.
El efecto del CYA en las tasas de desinfección se ha estudiado durante décadas. La lista de referencias adjunta proporciona un resumen de los diversos estudios que se han realizado a lo largo de los años con varios patógenos, incluyendo bacterias, virus, amebas y protozoos como el Cryptosporidium. En todos los estudios de tasas de eliminación publicados en revistas científicas revisadas por pares dentro del rango de pH de piscina de 7,2-7,8, se ha demostrado siempre que el tiempo que tarda el cloro libre en eliminar un organismo con ácido cianúrico es más largo que sin ácido cianúrico.
La dificultad radica en establecer un límite para el CYA y definir cuánto es demasiado. Dado que cada patógeno es único en su dosis infectiva, tasa de eliminación por cloro y otros factores, es difícil utilizar un criterio ‘único’ que pueda aplicarse a todos los patógenos y en todas las piscinas.
Se pueden utilizar los siguientes dos enfoques para ayudar a definir límites razonables:
Los Centros para el Control y la Prevención de Enfermedades (CDC) han realizado estudios que examinan el efecto del CYA en la eliminación del Cryptosporidium (crypto). El CDC no pudo lograr una reducción de 3 logaritmos (99,9%) con concentraciones de CYA superiores a 16 ppm. Por lo tanto, el CDC recomienda que para la remediación de un accidente fecal diarreico con cloro, la concentración de CYA debe estar por debajo de 15 ppm.
Para operaciones normales, entonces, el máximo de CYA podría establecerse en 15 ppm para que no sea necesario drenar el agua antes de responder a un accidente fecal diarreico.
Todos los desinfectantes de cloro para piscinas forman ácido hipocloroso (HOCl) cuando se disuelven en agua. Según se afirma en el Manual de Cloración de White, “esta especie de cloro es la más germicida de todos los compuestos de cloro, con la posible excepción del dióxido de cloro”iii. Como tal, la mayoría de las guías para operadores de piscinas, como el Manual para Operadores de Piscinas y Spas de la Fundación Nacional de Piscinas de Natacióniv, señalarán que el HOCl es la forma activa de cloro que elimina los microorganismos en el agua.
Utilizando las constantes de equilibrio químico conocidas, es posible calcular la concentración de HOCl con concentraciones crecientes de CYA. Los datos de la Agencia de Protección Ambiental (EPA) muestran que para eliminar la Giardia, se necesita 16,7 veces más monocloramina que cloro libre. La concentración calculada de CYA para reducir la concentración de HOCl en 16,7 veces puede determinarse en 14 ppm de CYA por 1 ppm de cloro libre disponible (FAC). Por lo tanto, para mantener la eficacia del FAC en comparación con la monocloramina, la relación CYA:FAC no debe exceder 14:1.
Si se mantienen niveles más altos de cloro, entonces se pueden utilizar niveles más altos de CYA, pero la relación CYA:FAC no debe ser superior a 14:1 para mantener la actividad del FAC al menos tan rápida como la de la cloramina. Por ejemplo, si se utiliza al menos 3 ppm de FAC, entonces 42 ppm (3 x 14) de CYA serían aceptables.
Utilizando las restricciones actuales de la EPA sobre las concentraciones de cloro (mínimo de 1 ppm y máximo de 4 ppm), se puede determinar el rango operativo aceptable de CYA.
Para una piscina donde hay grandes fluctuaciones en las concentraciones de cloro y se necesita el rango completo de 1-4 ppm de cloro, la concentración máxima de CYA debe ser de 14 ppm para asegurar que nunca se exceda la relación 14:1.
Para una piscina que puede mantener un control más estrecho y nunca permite que la concentración de cloro baje de 3 ppm, la concentración máxima de CYA anteriormente mencionada sería de 42 ppm para asegurar que nunca se exceda la relación 14:1.
A continuación se presenta una discusión más detallada de estos temas.
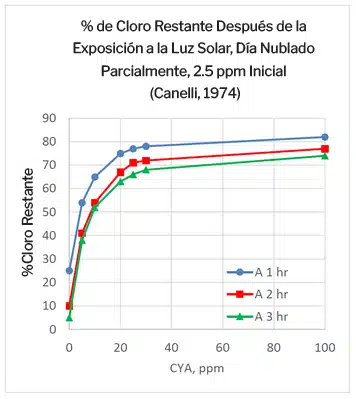
El efecto del CYA en la estabilización del cloro es bien conocido y se enseña en la mayoría de los cursos de formación para operadores de piscinas. El CYA se utiliza para estabilizar el cloro frente a la degradación provocada por la radiación UV de la luz solar. El siguiente gráfico muestra el porcentaje de cloro restante después de la exposición a la luz solar durante períodos de 1 hora, 2 horas y 3 horas.
El gráfico muestra que el efecto del CYA no es lineal, observándose la mayor mejora en la retención de cloro con los primeros
5 ppm de CYA. Sin CYA, solo el 25% del cloro permaneció después de una hora de exposición a la luz solar. Añadiendo solo 5 ppm de CYA, la retención de cloro aumentó al 54% después de una hora. La retención aumentó al 65% y 75%, después de una hora, para 10 ppm y 20 ppm de CYA, respectivamente. Se observó muy poco beneficio adicional al aumentar las concentraciones de CYA hasta 100 ppm para tiempos de exposición de 1 hora, 2 horas o 3 horas.
Para comprender el efecto del CYA en la desinfección, es importante entender la química del cloro y del CYA.
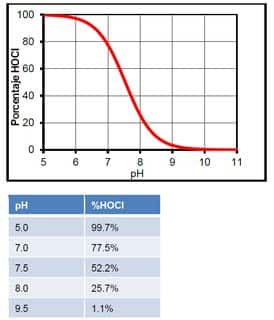
La cantidad de HOCl en el agua está gobernada por el pH debido al siguiente equilibrio:
En el agua, el HOCl puede dividirse en iones hipoclorito (OCl-) e iones de hidrógeno (H+). La cantidad que se divide dependerá del pH. A pH bajo, habrá más HOCl. A pH alto, habrá más OCl-. El %HOCl se muestra en el siguiente gráfico y tabla.
El ion hipoclorito no es tan eficaz en la eliminación de patógenos como el HOCl. Por lo tanto, es ventajoso asegurar que el pH no supere los 7,8, ya que obstaculizará la eficacia del cloro.
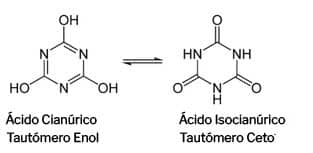
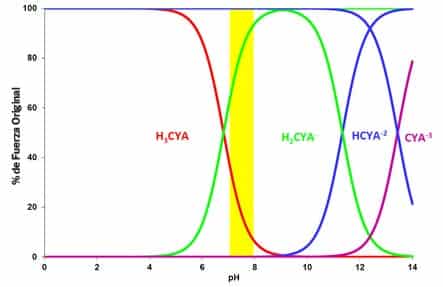
De manera similar al HOCl, los iones de hidrógeno pueden desprenderse de la molécula en el agua y la disociación depende del pH. El siguiente gráfico muestra el CYA y sus tres formas disociadas frente al pH.
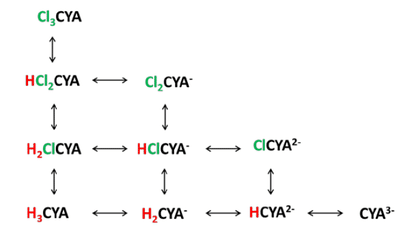
Dado que el CYA puede unirse hasta a tres iones de hidrógeno o tres átomos de cloro, los equilibrios pueden ser complejos. A continuación se muestra una figura que ilustra estos equilibrios.
A finales de la década de 1960 y principios de la de 1970, un estudiante de posgrado de Harvard, Joseph O’Brien, midió los equilibrios entre estas especies y publicó constantes de equilibrio para estas reaccionesxi. Estas constantes de equilibrio pueden utilizarse para calcular la cantidad de cada especie presente en condiciones determinadas.
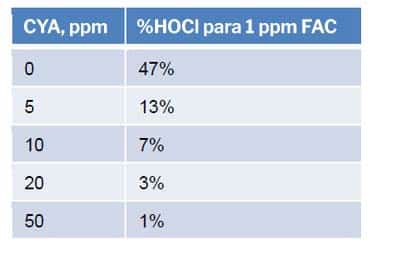
Considerando el ejemplo de una piscina con un FAC de 1 ppm (FAC medido con un kit de prueba de piscina típico) y un pH de 7,5, la concentración de HOCl variará según la concentración de CYA. Para una piscina sin CYA, el contenido de HOCl es de 0,52 ppm, mientras que una piscina con 50 ppm de CYA tendría un contenido de HOCl de 0,01 ppm.
Mediante estos cálculos, es fácil observar que hay menos HOCl, la forma activa del cloro, disponible en presencia de CYA.
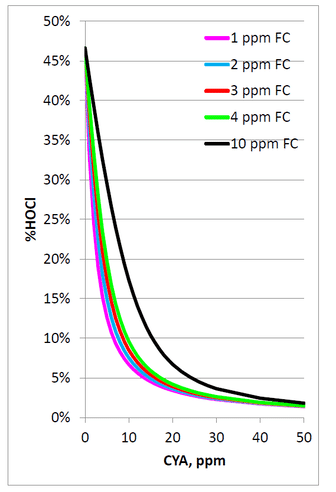
El siguiente gráfico y tabla muestran el porcentaje de HOCl para varias concentraciones de FAC con pH 7,5, 800 ppm de sólidos disueltos totales (TDS) y una temperatura de 85°F.
Estos datos demuestran claramente que el aumento de las concentraciones de CYA conducirá a una disminución de las concentraciones de la forma activa del cloro, HOCl.
Aunque el mundo práctico no se adhiere estrictamente a esta lógica, en general, niveles más elevados de un biocida (es decir, algo que mata organismos vivos) matarán las cosas más rápidamente. Si se utilizan niveles más bajos, tardará más tiempo.
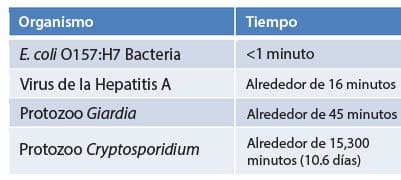
El CDC ha publicado algunos valores CT típicos del cloro en su sitio web de natación saludable (www.healthyswimming.org). Estos valores también están disponibles en el Anexo del Código Modelo de Salud Acuática (MAHC) del CDC. Los valores son para pruebas realizadas con 1 ppm de FAC a pH 7,5, 77°F y sin CYA.
Estos datos muestran que las bacterias como E. coli son relativamente fáciles de matar – 1 ppm de FAC generalmente puede matarlas en menos de un minuto. Crypto es un asunto completamente diferente. Incluso si una piscina se mantiene a 1 ppm de cloro libre, el crypto puede sobrevivir durante más de 10 días.
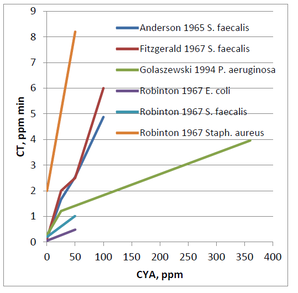
Como cabría esperar de las concentraciones reducidas de HOCl en presencia de CYA, las tasas de eliminación de los organismos son más lentas. A continuación se muestra un gráfico de valores CT que resume varios conjuntos de datos sobre bacterias publicados en los años 60
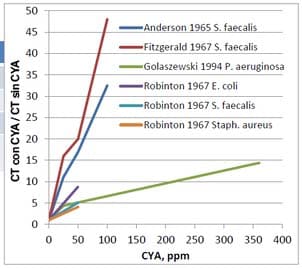
La comparación de la relación de estos valores CT (CT con CYA/ CT sin CYA) frente al CYA permite una comparación más relativa en el cambio del valor CT.
Utilizando este segundo gráfico, el impacto en el aumento relativo del valor CT es mucho más evidente. Por ejemplo, Fitzgerald observó un incremento de más de 45 veces en el valor CT en presencia de 100 ppm de CYA.
Para todos los diferentes investigadores que analizaron los diversos organismos, es evidente a partir del primer gráfico que los valores CT aumentan con el incremento de las concentraciones de CYA. Sin embargo, las líneas no se superponen completamente. Basándose en estos datos, es imposible hacer una afirmación general como ’50 ppm de CYA siempre causarán un aumento de 10 veces en el valor CT’. Eso podría ser cierto para los datos de E. coli generados por Robinton. No obstante, los datos de Pseudomonas aeruginosa generados por Golaszewski muestran un aumento de 5 veces, y los datos de Fitzgerald para Streptococcus faecalis muestran un aumento de 20 veces. Debido a las diferencias en los datos de las especies, es difícil hacer una afirmación definitiva con respecto a la concentración permisible de CYA en las piscinas.
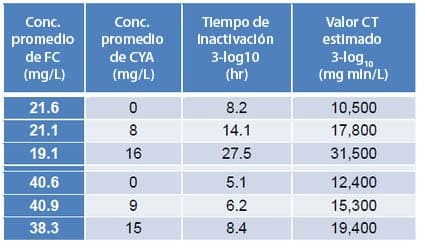
Una forma de estimar el nivel máximo permisible de CYA es examinar los datos del CDC sobre el criptosporidio. El CDC investigó el efecto del CYA en las tasas de eliminación del criptosporidio con cloro (Murphy 2015) de la siguiente manera:
Utilizando estos datos, el CDC estableció un protocolo de respuesta a accidentes fecales diarreicos. Este protocolo especifica que el nivel de CYA debe reducirse a 15 ppm para realizar la remediación, ya que el CDC no pudo obtener una reducción de 3 logaritmos del criptosporidio con más de 16 ppm de CYA.
Para evitar tener que drenar al menos parte de la piscina antes de realizar un tratamiento de remediación fecal con cloro, el nivel de CYA debería mantenerse por debajo de 15 ppm. La mayoría de la estabilización del cloro ocurre con dosis de CYA inferiores a 15 ppm. El aumento de la concentración de CYA tiene rendimientos decrecientes en la estabilización del cloro mientras incrementa los valores CT.
Otro enfoque para establecer una concentración máxima de CYA es comparar la actividad del cloro con la de la cloramina. La cloramina es utilizada por las instalaciones municipales de agua potable para desinfectar el agua. En esta aplicación, hay largos tiempos de residencia en el sistema de distribución de agua, por lo que un desinfectante de acción lenta es aceptable. Sin embargo, en una piscina donde los nadadores están en estrecha proximidad entre sí y se ha documentado la transmisión fecal-oral de enfermedades, se necesita un desinfectante de acción rápida para prevenir la transmisión de enfermedades de bañista a bañista. La cloramina no actúa con suficiente rapidez y, por lo tanto, no ha sido aceptada por la EPA como un desinfectante registrado para piscinas.
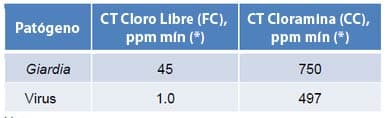
La siguiente tabla contiene valores CT de uno de los manuales de orientación de tratamiento de agua potable de la EPA. Como se observa en esta tabla, los valores CT para la monocloramina son mucho más altos que los del cloro libre. Para Giardia, la cloramina es 16,7 veces más lenta que el cloro libre (750/45 = 16,7). Para los virus, es 497 veces más lenta. En un sistema de tratamiento de agua potable, donde hay tiempo suficiente para la reacción dentro del sistema de distribución, estas tasas de eliminación más lentas son aceptables. Sin embargo, en un entorno de piscina, las cloraminas no se consideran desinfectantes suficientes.
Notas:
* pH 7,5, 25 °C, 3 log, 1 ppm FC
** pH 6-9, 25 °C, 3 log, 2-10 ppm monocloramina. La información sobre la concentración de 2-10 ppm de monocloramina se obtuvo del Manual de Orientación para el Cumplimiento de los Requisitos de Filtración y Desinfección para Sistemas Públicos de Agua que Utilizan Fuentes de Agua Superficial, EPA 1991.
Giardia es un patógeno relevante tanto para el agua potable como para el agua de piscina. En 1999, se enviaron al CDC muestras de heces formadas de piscinas cloradas para su análisis. Se encontró Giardia en el 4,4% de las muestras. Fuera de los accidentes fecales evidentes, se ha estimado que cada nadador libera un promedio de 0,14 g de material fecal al nadar. Los brotes de Giardia se informan regularmente en los resúmenes de vigilancia de brotes del CDC (Hlavsa 2015).
Los datos de la EPA sobre la inactivación de Giardia, donde la cloramina es 16,7 veces más lenta que el cloro libre, pueden tomarse como referencia para determinar el nivel de desinfección suficiente. En otras palabras, se debe mantener suficiente HOCl en el agua para garantizar que las tasas de eliminación de Giardia con cloro no sean más lentas que las tasas de eliminación de Giardia con monocloramina.
Desafortunadamente, las tasas de eliminación de Giardia son extremadamente difíciles de obtener debido al hecho de que el único medio fiable para obtener los datos requiere el uso de mamíferos vivos para probar la viabilidad de Giardia después de ser tratada con desinfectante. Si bien no se han realizado pruebas que estudien el efecto del CYA en la tasa de eliminación de Giardia con cloro, aún es posible estimar el efecto del CYA observando la concentración de HOCl a varias concentraciones de CYA.
La idea de que las tasas de eliminación de patógenos en presencia de CYA son directamente proporcionales a las concentraciones de HOCl ha sido propuesta por Engel (1983) en su trabajo con Naegleria gruberi xxiii. Gardiner concluyó que los datos sugieren fuertemente que la acción bactericida del cianurato clorado en sí, aunque presente en concentración mucho mayor que el HOCl, es insignificante. Los gráficos lineales de Saita de 1998 de las proporciones de supervivencia del poliovirus frente a la relación molar de CYA : cloro mostraron una relación similarxxii. Gardiner (1973) también demostró que el tiempo requerido para el 99% de eliminación de S. faecalis graficado frente a la relación de CYA : cloro resultó en una línea rectaxxiv. El trabajo de Gardiner, Saita y Engel muestra que para bacterias, virus y amebas, las tasas de eliminación en presencia de CYA son proporcionales a la concentración de HOCl, no a la concentración total de cloro libre.
Se utilizó el siguiente procedimiento para determinar el nivel máximo de CYA que puede usarse para garantizar que la tasa de eliminación no sea más lenta que 1 ppm de monocloramina (es decir, 16,7 veces más lenta que 1 ppm de cloro libre no estabilizado). Esto se hizo calculando el nivel máximo de CYA que asegurará que la concentración de HOCl no disminuya más de 16,7 veces la concentración sin CYA.
La concentración de HOCl puede calcularse utilizando las constantes de equilibrio publicadas por O’Brien. Utilizando los parámetros de química del agua de la tabla de la EPA anterior (pH 7,5, Temperatura 25°C, 1 ppm FAC) y un valor de TDS de 800 ppm, la concentración de HOCl es 0,360 ppm.
Basándose en los datos de Giardia de la EPA y para garantizar que la tasa de eliminación no sea más lenta que la monocloramina, el objetivo debería ser mantener una concentración de HOCl de al menos 0,360/16,7 ppm o 0,0216 ppm.
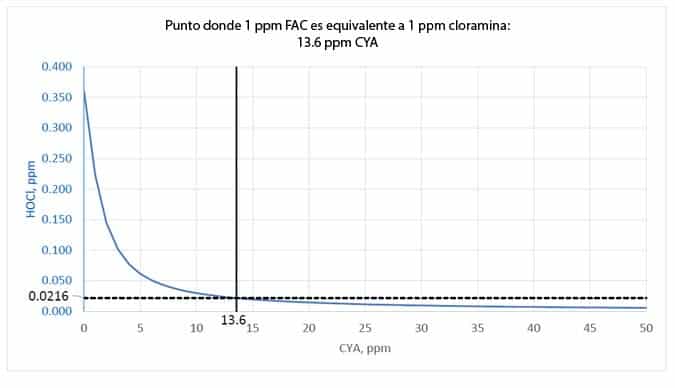
A continuación se presenta un gráfico de valores calculados utilizando las siguientes condiciones: pH 7,5, TDS 800 ppm, temperatura 25°C, 1 ppm FAC. La línea azul muestra la disminución de HOCl con el aumento de la concentración de CYA. El punto mencionado anteriormente donde la concentración de HOCl alcanza 0,0216 ppm es a 13,6 ppm de CYA.
Si la concentración mínima de cloro para piscinas estabilizadas y no estabilizadas es de 1 ppm, entonces el límite para CYA debería ser de 13,6 ppm para garantizar que el cloro no sea menos efectivo que 1 ppm de cloramina.
Sin embargo, el MAHC especifica que la concentración mínima de cloro para piscinas estabilizadas es de 2 ppm. Recalculando los valores utilizando 2 ppm FAC resulta en el siguiente gráfico.
El punto donde la concentración de HOCl (línea azul) alcanza 0,0216 ppm es a 28,1 ppm de CYA. Dado el mínimo de 2 ppm FAC en el MAHC, el nivel máximo permitido de CYA debería ser 28,1 ppm para garantizar que el cloro no sea menos efectivo que 1 ppm de cloramina.
Para mantener la eficacia del FAC en comparación con la monocloramina, la concentración de CYA no debe exceder los 14 ppm por cada ppm de FAC. Si se mantienen niveles más altos de cloro, entonces se pueden usar niveles más altos de CYA, pero la relación CYA:FAC no debe ser mayor que 14:1 para mantener la actividad del FAC al menos tan rápida como la de la cloramina. Por ejemplo, si se utiliza al menos 3 ppm de FAC, entonces 42 ppm (3 x 14) de CYA sería aceptable.
Utilizando las restricciones actuales de la EPA sobre las concentraciones de cloro (mínimo de 1 ppm y máximo de 4 ppm), se puede determinar el rango operativo aceptable de CYA.
Para una piscina donde existen grandes fluctuaciones en las concentraciones de cloro y se necesita el rango completo de 1-4 ppm de cloro, la concentración máxima de CYA debe ser de 14 ppm para garantizar que nunca se exceda la proporción de 14:1.
Para una piscina que puede mantener un control más estricto y nunca permite que la concentración de cloro descienda por debajo de 3 ppm, la concentración máxima de CYA mencionada anteriormente sería de 42 ppm para garantizar que nunca se exceda la proporción de 14:1.
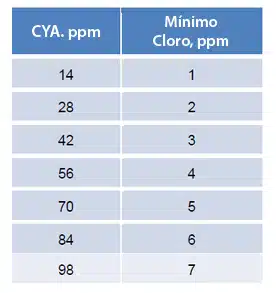
El MAHC permite concentraciones de cloro de hasta 10 ppm. La siguiente tabla muestra la concentración mínima de cloro que se requeriría para diversas concentraciones de CYA.
Dada una concentración de CYA de 70 ppm, la concentración mínima de cloro debería ser de 5 ppm. Dado que la concentración máxima de cloro según los CDC es de 10 ppm, esto permitiría que la piscina operara con concentraciones de cloro entre 5 y 10 ppm. Sin embargo, operar en este rango violaría las etiquetas de cloro de la EPA, que no permiten concentraciones de cloro superiores a 4 ppm en piscinas y 5 ppm en spas. Por lo tanto, para mantener las concentraciones de cloro en piscinas dentro del rango obligatorio de la EPA de 1-4 ppm y conservar la eficacia del cloro, el CYA debe mantenerse en no más de 14 ppm.
Si bien no es un problema de salud pública, las algas son ciertamente un problema para los propietarios de piscinas. En consecuencia, Lonza ha generado datos específicos para piscinas para determinar el efecto del CYA en el control de algas con cloro.
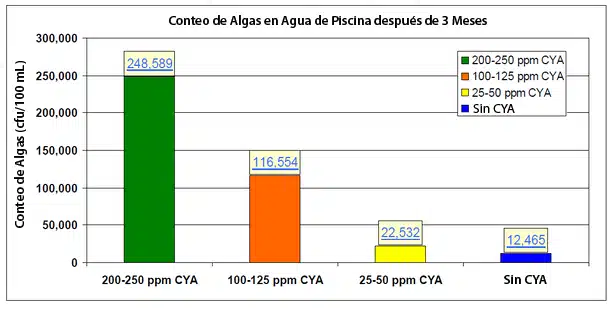
Se operaron ocho piscinas idénticas de 6,800 galones durante tres meses en una instalación de prueba en Miami, FL: dos piscinas de control sin CYA, dos piscinas con 25-50 ppm de CYA, dos piscinas con 100-125 ppm de CYA y dos piscinas con 200-250 ppm de CYA. Se añadieron algas y carga sintética de bañistas a las piscinas una vez por semana. Cada semana, 2 días después de las adiciones de contaminantes, las piscinas se trataban con un choque de 10 ppm de cloro disponible utilizando hipoclorito de calcio. El siguiente gráfico muestra que el aumento de las concentraciones de CYA condujo a un aumento en el recuento de algas.
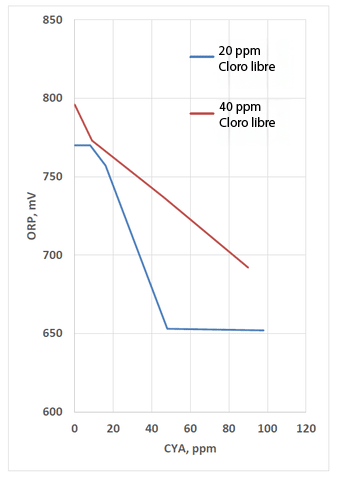
En el trabajo de los CDC con criptosporidio (Murphy 2015), se midió el ORP para varias combinaciones de cloro y CYA. Los resultados a continuación muestran que el aumento de CYA resulta en una disminución del ORP.
i Murphy, J.L., Arrowood, M. J., Lu, X., Hlavsa, M.C., Beach, M.J., Hill, V.R., 2015, Efecto del ácido cianúrico en la inactivación de Cryptosporidium parvum bajo condiciones de hipercloración, Environmental Science and Technology, 49(12), 7348-7355.
ii Código Modelo de Salud Acuática, Centros para el Control y la Prevención de Enfermedades, 2016.
iii G. C. White, Manual de Cloración, Segunda Edición, Van Nostrand Reinhold Company, Nueva York, 1986, página 153.
iv Manual del Operador de Piscinas y Spas, Fundación Nacional de Piscinas, Colorado Springs Co, 2017.
v O’Brien, J. E. Morris, J. C., Butler, J. N., Equilibrios en soluciones acuosas de isocianuratos clorados, En: Tratamiento Químico del Suministro de Agua, Capítulo 14, pp. 333-358; editado por A. J. Rubin, Ann Arbor Sciences, Ann Arbor, MI 1974. Presentado en el Simposio del Distrito, Filadelfia, 1973.
vi EPA LT1ESWTR Perfil y Evaluación Comparativa de Desinfección, 2003 EPA 816-R-03-004
viii Canelli, E.D., Propiedades químicas, bacteriológicas y toxicológicas del ácido cianúrico e isocianuratos clorados aplicados a la desinfección de piscinas, una revisión, AJPH Febrero 1974, 64(2) 155-162.
ix Constante de disociación de G. C. White, Manual de Cloración, Segunda Edición, Van Nostrand Reinhold Company, Nueva York, 1986
x O’Brien, J. E. Morris, J. C., Butler, J. N., Equilibrios en soluciones acuosas de isocianuratos clorados, En: Tratamiento Químico del Suministro de Agua, Capítulo 14, pp. 333-358; editado por A. J. Rubin, Ann Arbor Sciences, Ann Arbor, MI 1974. Presentado en el Simposio del Distrito, Filadelfia, 1973.
xi O’Brien, J. E., Equilibrios de hidrólisis e ionización del isocianurato clorado en agua, Tesis Doctoral, Cambridge, MA: Universidad de Harvard, 1972.